更新时间:2016-04-22 17:04 浏览: 次 作者:admin 文章来源:未知
NF-kB信号通路与细胞增殖、炎症、生存、变化密切相关。在NF-kB蛋白家族中,NF-kB p65的作用最为人熟知。当p65进入核内后,可以促进基因的转录,促进细胞生长和肿瘤演化。其中,最为常见的调控方式是,调控上游因子IKKα的磷酸化活性,促进IKB的磷酸化和泛素化降解过程,从而使p65从与IKB结合的复合体中释放出来,产生活性,促进靶基因的转录。本文根据近日刚发表在Cell期刊上的文章,围绕NF-kB信号通路的新的调控方式向您作展开介绍和解读。
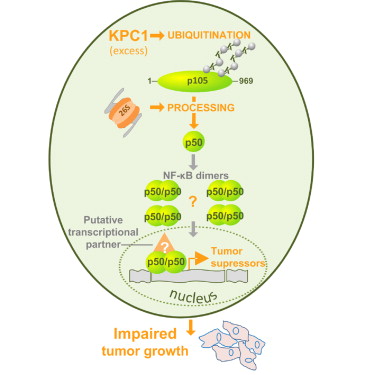
研究发现,KPC1具有泛素化连接酶活性,可以泛素化调节NF-kB1 p105,使之经蛋白酶降解,剪切后形成有活性的p50。p50可以促进肿瘤抑癌信号的表达,而且它的高表达可以下调p65,下调原癌基因的表达。此外,研究同时发现,与人正常组织相比,人肿瘤细胞中KPC1和p50表达下调,说明KPC1可调控p50而具有抑制癌症的作用。
1. KPC1具有调节p105泛素化的连接酶活性
通过裂解兔网状细胞后,将其裂解产物经分馏处理,并使用同位素标记的p105突变体(p105 S927A,不能被IKKβ磷酸化,也不能被βTreP所泛素化,排除βTreP所导致的泛素化),找到了可以泛素化p105的KPC家族。为了验证KPC能调节p105的泛素化,以标记的p105为底物,使用野生型和突变型的KPC1进行试验,说明KPC1的确可以调控p105泛素化,且该种调控方式属于特异性调控方式,即使是与p105同源性很高的p100也无法被泛素化。同时,在免疫共沉淀实验中发现,KPC1可以和p105结合,发生相互作用。说明KPC1很可能通过与P105结合发挥泛素连接酶活性,特异性调控p105泛素化。
2. KPC1可以促进p105程序性过程
在使用siRNA的放线菌酮实验中,研究人员发现,KCP1可以增加p50的产生,即促进p105生成p50。同时在使用野生型和突变型KPC1的实验中,证明了只有野生型的KPC1可以促进p105生成p50。此外免疫共沉淀实验结果显示,IKKβ不能改变p105 S927A与KPC1的结合,说明p105与KPC1的结合位点与IKKβ无关。再者,磷酸化的p105更易被KPC1泛素化,而非未磷酸化的p105。因此KPC1可以与磷酸化的p105结合发生相互作用,促进p50的产生,该过程不依赖于IKKβ。
3. KPC2在KPC1调节p105泛素化和程序化进程中的作用
KPC2是异质二聚体连接酶复合物中KPC1的一部分。在以p105为底物加入KPC1后加入KPC2,或者先加入KPC2再加入KPC1的实验中,结果显示KPC2具有去泛素化作用,且能被KPC1所恢复。它与KPC1泛素化p105的作用是相反的,且不会影响KPC1的表达。
4. p105与KPC1相互作用的位点
通过表达不同片段的p105和构建不同的p105突变体,来研究p105和KPC1的结合位点,研究人员找到了p105上的作用位点——锚蛋白重复序列C端。
5. KPC1或p50过表达对肿瘤生长的抑制作用
因为p50可以促进肿瘤抑癌基因的表达,抑制肿瘤生长,且前文中提到KPC1可以通过促进p105的泛素化过程而调控p50的产生,因此研究人员在下一步重点观察了KPC1或p50对肿瘤生长的影响。结果发现,在乳腺癌细胞MB-MDA 231、人骨肉瘤细胞U2OS、人脑星形胶质母细胞瘤U87-MG中,KPC1过表达可以显著抑制克隆形成率,然而突变型的KPC1(无泛素连接酶活性)却没有这种抑制效果。说明了KPC1通过其泛素连接酶活性可以抑制肿瘤细胞的生长。且敲除p105后,KPC1无法再促进p50的产生,也不能抑制肿瘤细胞的生长。且在动物荷瘤实验中,也说明了这一点。同时,KPC1处理后,会导致p65含量减少。因此,KPC1可以通过调控p105生成p50,同时也能降低p65的含量,从而抑制肿瘤细胞的生长。
6. KPC1对p50靶基因表达的调节作用
尽管KPC1可以通过调控p105来抑制肿瘤细胞的生长,但因此而影响到哪些基因的表达却在前文中没有提及,因此下一步研究人员针对KPC1对p50靶基因的表达影响进行了进一步的研究。通过基因芯片技术,研究人员检测了大量与肿瘤细胞相关的基因,包括凋亡相关基因、迁移相关基因及胞外基质相关基因等都发生了或上升或下调的显著变化。说明了KPC1的确可以调控p50靶基因的表达。
7. 人肿瘤、正常组织中KPC1与p50表达的相关性
然而,上述实验皆是在动物和细胞水平上进行的,并非以人体中的数据为依据。因此,研究人员又在人体中对相应指标进行了检测,从而为以上得出的结论提供了更为有力的证据。通过比较人正常组织和肿瘤组织中KPC1和核内p50的蛋白含量,发现肿瘤组织中KPC1和核内p50的含量兼比正常组织少。这验证了上述结果,即KCP1可以促进p105泛素化上调p50含量,从而抑制原癌基因的表达。而KPC1下调则会有相反的作用,下调p50,则会导致癌症的发生,所以在肿瘤组织中KPC1和p50的表达是下调的。
根据此项研究,研究人员发现了可以调控p105泛素化的新蛋白------KPC1,并发现了两者发生相互作用的位点和调控机制。KPC1可以促进p105产生p50,促进抑癌基因的表达,从而限制肿瘤细胞的生长,为肿瘤治疗提供了新的研究方向和潜在治疗靶点。(来源:百替生物 作者:朱萍亚)
原文摘要:
KPC1-Mediated Ubiquitination and Proteasomal Processing of NF-κB1 p105 to p50 Restricts Tumor Growth
NF-κB is a key transcriptional regulator involved in inflammation and cell proliferation, survival, and transformation. Several key steps in its activation are mediated by the ubiquitin (Ub) system. One uncharacterized step is limited proteasomal processing of the NF-κB1 precursor p105 to the p50 active subunit. Here, we identify KPC1 as the Ub ligase (E3) that binds to the ankyrin repeats domain of p105, ubiquitinates it, and mediates its processing both under basal conditions and following signaling. Overexpression of KPC1 inhibits tumor growth likely mediated via excessive generation of p50. Also, overabundance of p50 downregulates p65, suggesting that a p50-p50 homodimer may modulate transcription in place of the tumorigenic p50-p65. Transcript analysis reveals increased expression of genes associated with tumor-suppressive signals. Overall, KPC1 regulation of NF-κB1 processing appears to constitute an important balancing step among the stimulatory and inhibitory activities of the transcription factor in cell growth control.
扫一扫,获取更多医学科研最新资讯!
【Medical Research微信公众号】 【百替生物官方微博】

