更新时间:2016-12-06 09:03 浏览: 次 作者:admin 文章来源: 药明康德
今年,拉斯克基金会将基础医学研究奖授予了丹娜·法伯癌症研究所的威廉·凯林(William Kaelin)教授、牛津大学的彼得·拉特克利夫(Peter Ratcliffe)教授以及约翰霍普金斯大学的格雷格·塞门扎(Gregg Semenza)教授,以表彰他们在揭晓氧气相关信号通路上的贡献。


▲大卫·利文斯顿教授在威廉的科研道路上起到了决定性的作用(图片来源:丹娜·法伯癌症研究所)
在迷惘与困境中,大卫·利文斯顿(David Livingston)教授向威廉伸出了援手,将他纳入实验室。利文斯顿教授是视网膜母细胞瘤研究的先驱之一,在阐明这种癌症的机理上极有造诣。在利文斯顿教授的实验室中,威廉分离出了E2F蛋白,并发现它能够结合DNA,促进细胞增殖。在通常的情况下,E2F会被抑癌蛋白RB抑制,从而防止细胞过度分裂。然而当RB蛋白出现突变时,细胞就会不受控制地分裂,导致视网膜母细胞瘤的诞生。
这段意外的经历彻底改变了威廉的职业规划。在能同时接触癌症患者和一线癌症研究的情况下,威廉认识到“对这些患者来说,最终的希望还是来自对癌症分子机制的精准理解,以及由这些知识转化成的有效疗法。”
在1992年,威廉开设了属于自己的实验室。在寻找潜在的科研项目中,他了解到了一种叫做希佩尔-林道综合征(von Hippel-Lindau disease)的遗传疾病。这种疾病的患者会在肾脏,肾上腺、胰腺以及中枢神经系统等位置生出肿瘤。威廉注意到,这些肿瘤都生长在血管丰富的部位,而且它们会分泌促红细胞生成素,刺激红细胞的产生。这些特点都表明,氧气可能在它们的生长中起到了关键作用。
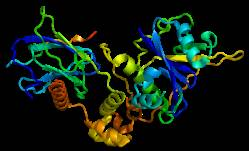
▲威廉发现了关键蛋白VHL的作用机理(图片来源:维基百科)
后续的研究结果也证明了这一点。当时,人们已经找到了和希佩尔-林道综合征相关的基因VHL。威廉的研究团队则发现在氧气充足时,VHL蛋白会标记一种叫做HIF的缺氧诱导因子,让它降解;而在氧气不足的情况下,VHL就失去了标记HIF的能力,因此HIF能继续留在细胞内起作用,并促进血管和红细胞的生成。
可是,这些细胞是怎么知道周围氧气是否丰富呢?
经过多年的探索,威廉与团队给出了答案:原来在氧气充足的情况下,细胞内羟化酶的效率会有所增加,使HIF蛋白获得一个羟基。而VHL能够识别这个羟基,并启动后续的调节功能。这项突破性的发现是人类首次意识到羟基化对于细胞信号通路有着至关重要的作用,它也因此刊登在了2001年的《科学》杂志上。

▲威廉团队在《科学》杂志上的论文,至今已被引用了3677次(图片来源:谷歌)
更重要的是,威廉的这个发现具有普适性。在多种疾病中,他的团队都发现了氧气在肿瘤形成过程中起到的作用。譬如肾癌患者的VHL基因往往会出现突变,导致人体内产生过量的VEGF(血管内皮生长因子),而这又会促进血管和红细胞的生成。基于这一原理,新药研发人员针对VEGF这一靶点开始研发新药。目前,FDA已经批准了多种用于治疗肾癌的VEGF抑制剂。
基于这项成就,威廉与另外两名独立发现同一信号通路机理的科学家一道分享了今年的拉斯克基础医学研究奖。然而对于威廉来说,这个奖项来得有些孤独——在以往,每当威廉收获荣誉,他的夫人卡罗琳都会陪伴在旁,和他一起分享喜悦。然而去年,身为乳腺癌医生的卡罗琳,却由于乳腺癌离开了这个世界。研究了一辈子癌症的威廉对此无能为力。

▲夫人的去世,是威廉心中永远的痛(图片来源:Boston Globe)
“她看到了自己的女儿从耶鲁大学毕业,见证了自己的儿子被耶鲁大学录取,也一同庆祝了我们的25周年结婚纪念日,”威廉说道:“当意识到生命的珍贵,它就变得丰富起来。”
爱妻的离去让威廉切身体会到癌症患者家属的痛苦,也让他越发明白基础研究的重要性。在工作之余,威廉也积极参与着促进癌症研究的工作——卡罗琳生前曾多次参加泛麻省公益自行车赛(Pan-Mass Challenge),以帮助丹娜·法伯癌症研究所募集经费。今年,威廉带着他妻子的遗愿,完成了这一挑战。
如今,只要能做出造福他人的新发现,威廉就会感受到幸福。至于荣誉,反倒成了身外之物。“只要你认真做科研,并一直问出好的问题,就不用太担心获奖的事情”,威廉说道。
参考资料:
[1] William G. Kaelin – HHMI
[2] Oxygen sensing – an essential process for survival
[3] Breast cancer surgeon turned patient, Carolyn Kaelin, dies at 54