更新时间:2016-04-22 17:06 浏览: 次 作者:admin 文章来源:未知
我国生物制药产业发展正处于快速上升期,而单克隆抗体药物无疑是其中表现最为活跃的组成。2011年,全球单抗药物的市场总量已经达到628亿美元,国内市场规模超过10亿元,并且每年以50%以上的速度递增,高于国际单抗市场的增长速度。
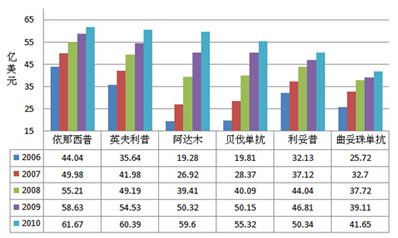
全球重磅单抗历年销售额
目前,我国的单克隆抗体产业已经形成了以北京、上海、西安以及武汉等产业化基地,而单克隆抗体也发展到了第四代,我国已经上市的十几个单抗药物多为鼠源性,正在研究中的多为嵌合或者人源化单抗,而全人源单抗还没有。而在全球的单克隆抗体市场,全人源化单克隆抗体是其未来的发展方向。在FDA批准上市的80多种基因工程和抗体工程产品中,抗体类产品有26种,其中18种为人源化抗体。目前基本上所以有关抗体的制药技术都被欧美国家垄断,致使国内制药企业在抗体药物研发方面备受掣肘。2012年10月23-24日,"2012生物制药工程论坛"在上海万豪虹桥大酒店召开,近二十位嘉宾就生物制药工程工艺发表了精彩的演讲,围绕生物制药研发和生产过程中的技术要点、生产关键工艺等问题与参会者展开了深入探讨。大家一致认为:我国抗体药物产业化的主要限制因素有三个方面:动物细胞大规模培养、抗体大规模纯化及药物质量分析和质量保证。
动物细胞大规模培养技术已成为各个国家生物医药产业化的核心竞争点
动物细胞大规模培养技术在抗体、重组蛋白和病毒疫苗等生物医药产品的研发和工业化生产中具有广泛的应用,动物细胞表达药物已经成为当今生物医药产业发展的主流。由于动物细胞表达产品需求的紧迫性和生产工艺的复杂性,大大促进了动物细胞大规模培养技术的深入研究与发展。当前动物细胞大规模培养技术已成为各个国家生物医药产业化的核心竞争点。
动物细胞大规模培养生产蛋白或抗体的工艺选择,应综合考虑产品特点、工艺难度与工艺研发时间,以加速其产品产业化的进程。当前,在被FDA批准的生物技术产品以及公开发表的生产工艺中,占有主流优势的是搅拌式生物反应器悬浮培养,工艺设计是流加或灌流培养。其大规模细胞培养生产所面临的挑战是:获得最大生产力的同时注重维持产品的质量,去除所有培养环境中外源因子的污染,更为精确有效的工艺控制手段,规模化培养中氧气的限定与溶解CO2 浓度累积的控制等。
我国动物细胞工程行业起步晚,目前上市产品数量和种类少,工程细胞株表达水平低,工业化生产规模小,最大规模只有3000L。华东理工大学生物反应器工程国家重点实验室谭文松教授在"2012生物制药工程论坛"演讲中指出:“我国动物细胞生物医药产业面临诸多瓶颈,如细胞培养生产工艺技术落后,受产能和成本制约严重;无血清培养基、生物反应器和原辅料等过分依赖进口;表达产物质量低,标准缺失;分工不够明确,产学研用合作严重不足,对相关人才培养和储备远远不够。而根本问题在于忽视工程问题,轻视工程研究。”
针对如上问题,谭教授也提出了自己的建议,他认为:“我国应该致力于各种无血清无蛋白培养基开发和生产,加大力度进行工程细胞株的代谢工程改造以早日拥有真正属于中国的CHO工程细胞,也需加强对细胞培养过程的理解和优化,提高抗体表达速率,开发高产量、高质量的细胞培养工艺。在生物反应器放大和强化技术方面,应致力于突破千升级、万升级动物细胞生物反应器的设计、制造和操作,重视培养过程计算机实时监测和控制技术,更好地理解生物反应器中的代谢规律,满足高密度培养过程的需要。”
北京天广实生物技术有限公司副总经理叶培在报告中也提到,在动物细胞大规模培养工艺开发过程中,需要从生产过程工艺、培养条件参数设置和罐体控制三个方面进行优化,包括设备的配置、搅拌桨设计、sparger选择和流加条件、溶解氧、气体流量、代谢产物等方面,是一个涉及到生物、化工、机械等的综合学科知识。
抗体下游纯化成本已占45%到70% 高质量纯化工艺研究刻不容缓
随着越来越多的生物药物得到批准和投入生产,临床使用量达到数十到数百毫克,对生产制造纯化工艺的效能和成本要求也越来越高。生物技术药物产业的发展对生产制造规模和产品纯度的要求也越来越严格。
据统计,抗体药物开发的60%资金投入都在下游纯化工艺的建立,药物制造成本可达到售价的20-25%。上海交通大学生物制造实验室主任李荣秀教授指出:“细胞培养产率从0.1g/L 提高到1g/L ,可以引起下游纯化成本比例从45%到70%,这是所有生物制药企业不可忽视的一个环节。生产中可以减少纯化步骤, 缩短生产周期,降低生产成本, 提高生产效率,将在生物技术药物制造纯化方面发挥重要作用。”
嘉和生物药业有限公司产品及工艺研发部总监李晓辉认为:“抗体药物下游纯化工艺的开发是一个复杂的过程,需要综合考虑纯度、收率、成本、时间等因素。”
抗体药物质量分析:QbD(质量源于设计)理念重要性凸显
抗体药物质量检测标准的建立和验证是药物最终获得批准进入生产流通的核心环节,目前我国还没有完全形成标准,需要学术界和产业界积极配合共同制定符合标准的抗体药物质量标准。
上海药明康德新药开发有限公司蛋白质分析及生物分析服务执行主任王少雄博士在报告中提到:“根据目前美国FDA通用的QbD理念,质量分析检测需要贯穿整个过程,对最终产品有着至关重要的影响。在抗体药物研发过程中,从细胞株构建、细胞工艺开发、纯化和制剂等环节都需要进行严格的检测,包括蛋白A 高效液相法色谱滴度分析,糖基化分析,聚体分析、肽图、结合力分析、效价分析、宿主细胞DNA、残留细胞DNA、残留蛋白A等的检测。”
在制药技术发展及“十二五”医药生物产业相关规划的推动下,我国抗体产业发展迅速,"2012生物制药工程论坛"演讲嘉宾们也纷纷看好抗体药物发展前景,上海药明康德新药开发有限公司副总裁陈智胜更直言:“中国生物药平台已非常成熟,在接下来的两到三年里,中国会出现世界上最新的一个单克隆抗体产品。” (生物谷 Bioon.com)